پویایی شیمیایی و تعادل شیمیایی
شیمی به عنوان علمی که در بررسی ساختار، خصوصیات و تغییرات ماده مشغول است، محدودهای گسترده از پدیدهها و فرآیندهای مختلف را پوشش میدهد. با گذشت دویست سال از اکتشافات و پیشرفتهای چشمگیر در این حوزه، مسائلی از قبیل پویایی شیمیایی و تعادل شیمیایی همچنان تحت توجه قرار دارند. در این مقاله، ما به بررسی ارتباط بین این دو مفهوم اصلی در علم شیمی، یعنی پویایی شیمیایی و تعادل شیمیایی میپردازیم و نقش آنها در فرآیندهای شیمیایی را مورد بررسی و تجزیه و تحلیل قرار میدهیم.
مفهوم پویایی شیمیایی
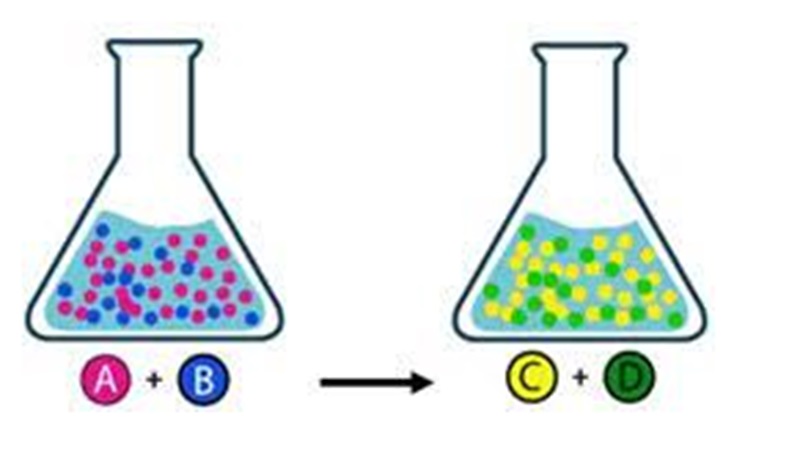
پویایی شیمیایی به واکنشها و تغییراتی اطلاق میشود که در طول زمان رخ میدهند و مواد شیمیایی را از یک حالت به حالت دیگر تبدیل میکنند. این تغییرات میتوانند به صورت تدریجی و آهسته یا به صورت سریع و فوری اتفاق بیفتند. در پویایی شیمیایی، مولکولها و یونها به طور مداوم با یکدیگر تعامل میکنند و واکنشهای شیمیایی اتفاق میافتند که منجر به تشکیل محصولات جدید میشود. این واکنشها ممکن است با حرارت، فشار، نور، یا حتی بدون نیاز به هیچ گونه عامل خارجی دیگری اتفاق بیفتند.
مهمترین جنبههای پویایی شیمیایی عبارتند از:
۱. سرعت واکنش: سرعت واکنشهای شیمیایی میزان تغییرات مولکولی در یک واکنش را نشان میدهد. این سرعت ممکن است به وابستگی از عواملی مانند دما، فشار، و غلظت مولکولها تغییر کند.
۲. تعادل شیمیایی: در برخی از واکنشهای شیمیایی، مولکولها به تعادل میرسند، به این معنا که نرخ واکنش به سمت جلو برابر با نرخ واکنش به سمت عقب میشود. این وضعیت تعادل باعث میشود تا مقادیر مواد واکنشی در طول زمان ثابت بمانند، اما واکنش همچنان ادامه دارد.
۳. تعاملات مولکولی: پویایی شیمیایی همچنین شامل تعاملات مولکولی مختلف است که منجر به تشکیل پیوندهای شیمیایی جدید، شکلدهی مولکولهای جدید، و تغییر شکل مولکولها میشود.
به طور کلی، پویایی شیمیایی مفهومی است که بر روی تغییرات واکنشی در مولکولها و اتمها تمرکز دارد و نقش اساسی در فرآیندهای شیمیایی و زندگی دارد.
مفهوم تعادل شیمیایی
تعادل شیمیایی وضعیتی است که در آن نرخ واکنش به سمت جلو برابر با نرخ واکنش به سمت عقب میشود. به عبارت دیگر، در یک تعادل شیمیایی، میزان مواد واکنشی در یک وضعیت ثابت میماند و به نظر میرسد که واکنش متوقف شده است، اما در واقع، واکنش همچنان ادامه دارد. تعادل شیمیایی معمولاً در واکنشهایی که انجام آنها در دما و فشار ثابت انجام میشود، بروز میکند.
مهمترین ویژگیهای تعادل شیمیایی عبارتند از:
۱. حالت ثابت: در یک تعادل شیمیایی، مقدار مواد واکنشی در حالتی ثابت باقی میماند. این به این معناست که تعداد مولکولهای مواد موجود در وضعیت تعادلی ثابت میماند.
۲. نرخ واکنشها: در تعادل شیمیایی، نرخ واکنش به سمت جلو برابر با نرخ واکنش به سمت عقب میشود. این به این معناست که در هر لحظه، مولکولها از یک سمت به سمت دیگر حرکت میکنند.
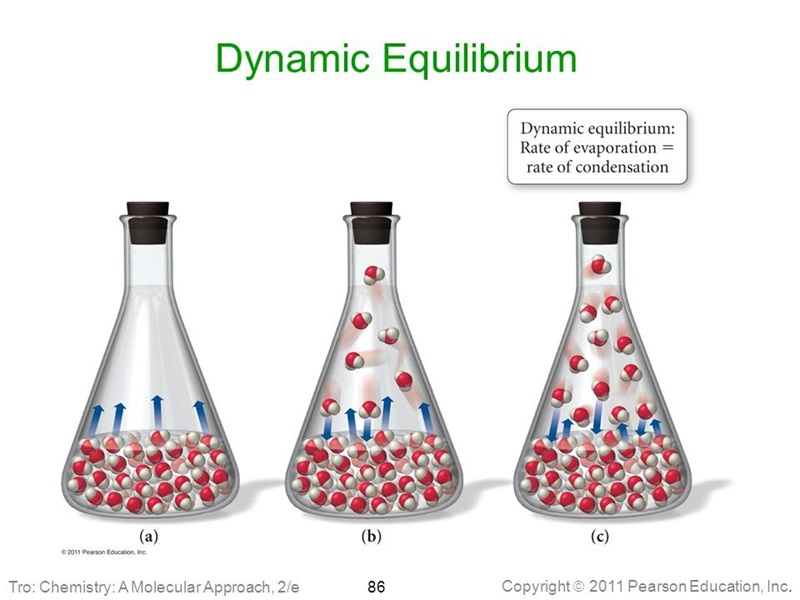
۳. تعادل دینامیکی: تعادل شیمیایی یک حالت دینامیکی است که در آن واکنش همچنان ادامه دارد، اما در یک نرخ ثابت و بدون تغییر میزان مواد واکنشی.
تعادل شیمیایی در موارد مختلفی از علم شیمی و بیولوژی مشاهده میشود و در فرآیندهایی مانند تشکیل آمینواسیدها در بدن، تشکیل آب در واکنشهای شیمیایی، و تشکیل اسیدها و بازها در محلولهای آبی نقش مهمی ایفا میکند.
ارتباط بین پویایی شیمیایی و تعادل شیمیایی
پویایی شیمیایی و تعادل شیمیایی دو جنبه مهم و مرتبط در علم شیمی هستند که با هم ارتباط دارند. این دو مفهوم از طریق فرآیندهای شیمیایی و واکنشهای شیمیایی با یکدیگر تعامل دارند و در برخی موارد، به طور مستقیم به یکدیگر وابسته هستند.
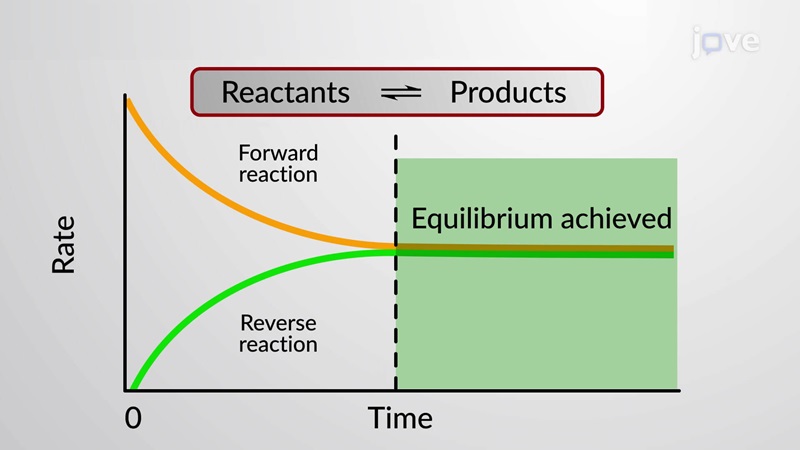
۱. پویایی شیمیایی و تعادل: در بسیاری از واکنشهای شیمیایی، پویایی و تعادل با یکدیگر تلاقی میکنند. به عنوان مثال، در یک واکنش شیمیایی که به تعادل میرسد، هر دو جهت واکنش (واکنش به سمت جلو و واکنش به سمت عقب) همزمان ادامه دارد. این به این معناست که مولکولها همچنان در حرکت هستند و واکنش پویایی شیمیایی ادامه دارد، اما در نهایت، واکنش به یک تعادل شیمیایی میرسد که در آن نرخ واکنش به سمت جلو برابر با نرخ واکنش به سمت عقب میشود.
۲. تأثیر شرایط محیطی بر پویایی و تعادل: شرایط محیطی مانند دما، فشار، و غلظت مواد واکنشی میتوانند بر پویایی و تعادل شیمیایی تأثیر بگذارند. به عنوان مثال، افزایش دما معمولاً باعث افزایش نرخ واکنش میشود، که میتواند به تعادل جدیدی منجر شود. همچنین، تغییرات در فشار و غلظت نیز میتوانند به تغییرات در تعادل شیمیایی و پویایی واکنشها منجر شوند.
در کل، پویایی شیمیایی و تعادل شیمیایی دو مفهوم مرتبط هستند که هر دو نقش مهمی در فرآیندهای شیمیایی ایفا میکنند و درک عمیق از این دو مفهوم میتواند به ما کمک کند تا فرآیندهای شیمیایی را بهتر درک کرده و کنترل کنیم.


دیدگاهتان را بنویسید