مبحث ترمودینامیک فیزیک دبیرستان

ترمودینامیک هم به بررسی تغییرات انرژی درونی یک سیال میپردازد. این سیال میتواند هوا در یک اتاق، یا حتی کل اتمسفر زمین، یک لیوان چای یا حتی آب در تمامی اقیانوسهای سطح زمین باشد.
مبحث ترمودینامیک فیزیک دبیرستان کتب درسی دوره یازدهم. معمولا ما تاکید داریم که ماده مورد مطالعه را بهعنوان یک گاز محصور و منعزل محدود میکنیم تا محاسبات سادهتری داشته باشیم.
تغییر وضعیت در علم ترمودینامیک به معنای تغییر و تبادلات انرژی درونی یک گاز با ویژگیهای خاص است که باید بررسی شود. هر گازی دارای مقداری انرژی درونی است، که مجموع انرژی پتانسیل و جنبشی تمام ذرات یک گاز است و با حرف U نمایش داده میشود.
برای ترمودینامیک محاسبه انرژی جنبشی ذرات، به دانستن سرعت ذرات تکی نیاز داریم. (که عملی غیر ممکن است) تا بتوانیم انرژی جنبشی هر ذره را محاسبه و آنها را باهم جمع کنیم . تا به مقدار انرژی جنبشی تمام ذرات اتم برسیم. هنوز انرژی پتانسیل ذرات را محاسبه نکردهایم.
این روش بررسی تغییرات یک گاز به عنوان روش میکروسکوپیک شناخته میشود، زیرا در این روش با مقادیر کوچک مقیاس سر و کار داریم. استفاده از این روش نیازمند دانش ریاضی و فیزیک پیشرفته است.
همچنین، روش ماکروسکوپیک دیگری نیز وجود دارد که در آن با کمیتهای بزرگ مقیاس کار میکنیم. کمیتهایی مانند فشار (P)، دما برحسب مقیاس کلوین (T)، حجم (V) و تعداد مول (n) یک ماده.
در روش ماکروسکوپیک. برای بررسی تغییر انرژی درونی یک گاز (ΔU)، کافی است تبادلات انرژی گرمایی (Q) و کار (W) را بین گاز مورد نظر. و محیط اطراف آن بررسی کنیم. یعنی به جای اینکه انرژی درونی یک گاز را در دو حالت مختلف بدانیم و آنها را از هم کم کنیم، میتوانیم میز

گاز کامل (ایده آل – آرمانی)
اگر کلاس درسی با 50 دانشآموز را در نظر بگیریم و چند دوربین در جاهای مختلف کلاس قرار دهیم تا رفتار دانشآموزان را بررسی کنیم، خواهیم دید که الگوهای مختلفی از رفتار و تمرکز بر درس وجود دارد. برای مثال، بعضی از دانشآموزان در ردیفهای اول و دوم به درس گوش میدهند، ردیفهای سوم و چهارم احتمالا در حال صحبت و پچپچ با یکدیگر هستند و دانشآموزان ردیف آخر ممکن است در بهترین حالت، خوابیده باشند.
این الگوهای رفتاری را میتوان با مولکولهای یک گاز در یک ظرف قرار داده شده مقایسه کرد. اگر چند دماسنج و فشارسنج در انواع مختلف گاز در نقاط مختلف ظرف قرار داده شود، هر یک از این ابزارهای اندازهگیری نتایج متفاوتی را نشان میدهند که ناشی از اختلاف انرژی در نقاط مختلف گاز است.
اگر تعداد دانشآموزان را به 5 نفر کاهش دهیم، ممکن است تمام دانشآموزان در حال تمرکز بر روی معلم و درس باشند. به همین ترتیب، اگر غلظت گاز را کاهش دهیم و از برهمکنش بین مولکولها و دیواره ظرف چشمپوشی کنیم، میتوانیم به یک وضعیت مشابه در گاز دستیابیم که تمام مولکولهای آن در دما، فشار و انرژی مشابهی قرار دارند.
این وضعیتی است که در مورد گاز آرمانی یا ایدهآل صادق است که به عنوان یک مدل سادهتر از گاز واقعی شناخته میشود و در برخی کتابهای درسی دانشگاهی به اسم گاز کامل یا ایدهآل مطرح میشود.
دستگاه
گاز را در مخزنی حبس میکنیم و تبادلات انرژیِ آن را با محیط بیرون این مخزن بررسی میکنیم ، از این به بعد به گاز حبس شده دستگاه میگوییم . در بیشتر مسائل مخزن به شکل پیستونی در نظر گرفته می شود تا در صورت لزوم بتوانیم حجم گاز را تغیر دهیم .
محیط
هر آنچه که دستگاه را احاطه کرده و با آن تبادل انرژی دارد، به عنوان محیط شناخته میشود.
محیط به گونهای انتخاب میشود که دمای آن با تغییرات دمای دستگاه تغییر نکند. به عبارت دیگر، افزایش یا کاهش دمای دستگاه و یا تبادل انرژی بین محیط و دستگاه، تأثیری در دمای محیط نداشته باشد. با این حال، با تغییر دمای محیط میتوانیم دمای دستگاه را تغییر دهیم.
به عنوان مثال، یک لیوان چای، هر چقدر هم داغ باشد، قادر نیست دمای اتاق را افزایش دهد. به همین ترتیب، یک پارج آب یخ نیز نمیتواند دمای اتاق را کاهش دهد. بنابراین، میتوان لیوان چای داغ یا پارج آب یخ را به عنوان دستگاه و اتاق را به عنوان محیط در نظر گرفت.
حالت ترمودینامیکی
منظور از حالت ترمودینامیکی ، وضعیت گاز از لحاظِ کمیت های ترمودینامیکی است ، یعنی فشار ، دما ، حجم و تعداد مول گاز چقدر است و چه رابطه این بین این کمیتها وجود دارد.
تعادل ترمودینامیکی
اگر فشار و دمای مطلق یک گاز کامل، در همه نقاط آن گاز کامل و منزوی یکسان باشد، به اصطلاح، گاز در وضعیت تعادل ترمودینامیکی قرار دارد. این نکته حائز اهمیت است که تعادل ترمودینامیکی به معنای برابری بین کمیتهای ترمودینامیکی نیست، زیرا هر کدام از این کمیتها واحدهای متفاوتی دارند. تعادل ترمودینامیکی به این معناست که همه مولکولهای یک گاز کامل، انرژی یکسانی دارند.
معادله حالت
هنگامی که یک گاز کامل در وضعیت تعادل ترمودینامیکی قرار دارد، بین کمیتهای فیزیکی مانند فشار (P)، دما (T)، حجم (V)، و تعداد مول (n) یک گاز کامل رابطهای وجود دارد که به آن “معادله حالت گاز کامل” یا به اختصار “معادله حالت” میگویند.
در این رابطه، T دمای مطلق گاز به واحد کلوین و R ثابت عمومی گازهاست، که مقدار آن برابر 8/3 است. به منظور سادگی محاسبات، اغلب مقدار R را برابر 8 در نظر میگیریم.
فرآیند ترمودینامیکی
تغییر وضعیت گاز کامل از یک حالت تعادل به حالت تعادل جدید را فرآیند ترمودینامیکی میگویند. یعنی گاز از فشار (P1) ، دما (T1) و حجم (V1) اولیه به فشار (P2) ، دما (V2) و حجم (T2) متفاوتی میرسد، در طی یک فرآیند ترمودینامیکی، ممکن است یک، دو و یا هر سه کمیت تغییر کند
فرآیند ایستاوارِ ترمودینامیکی
اگر در طول یک فرآیند ترمودینامیکی، وضعیت گاز به طور مداوم به حالت تعادل نزدیک شود، آن فرآیند به عنوان فرآیند استوار شناخته میشود. به طرز سادهتر، در طول یک فرآیند ترمودینامیکی، هر زمان که کمیتهای ترمودینامیکی یک گاز را اندازه میگیریم، معادله حالت برای آنها همواره باید برقرار باشد.
انواع فرآیندهای ترمودینامیکی
در کتاب فیزیک دهم دبیرستان چهار نوع از فرآیندهای ترمودینامکی ایستاوار را بررسی خواهیم کرد:
فرآیندهای هم حجم ، هم فشار ، هم دما و بی در رو
محاسبه گرما
در فصل ترمودینامیک کتاب درسی، روابط مربوط به محاسبه گرما حذف شده است. در اینجا، فقط نشانههای مربوط به آنها را بررسی خواهیم کرد. بعدها، روش محاسبه گرما را در بخش دیگری برای علاقهمندان توضیح خواهیم داد.
هر زمان که گرما به دستگاه وارد میشود، مقدار گرما مثبت است و هر زمان که گرما از دستگاه خارج میشود، مقدار آن منفی است. به عبارت دیگر، اگر محیط به دستگاه گرما بدهد، آنگاه Q>0 خواهد بود و اگر دستگاه به محیط گرما بدهد، آنگاه Q<0 خواهد بود.
محاسبه کار
کار در فرآیندهای ترمودینامیکی از رابطه زیر محاسبه میشود:
[ W = -P \Delta V ]
در اینجا، P نمایانگر فشار است که برحسب واحد پاسکال است و ΔV تغییر حجم گاز را برحسب واحد مترمکعب نشان میدهد. لازم به ذکر است که وجود یک علامت منفی در سمت راست معادله، نشاندهنده این است که علامت کار همیشه با تغییرات حجم قرینه است. به این معنا که در فرآیندهای انبساطی که حجم گاز افزایش مییابد، کار منفی است و در فرآیندهای انقباضی که حجم گاز کاهش مییابد، علامت کار مثبت است.
فرآیند هم حجم
در این فرآیند، حجم گاز ثابت میماند و با تغییر دما، فشار آن تغییر میکند. با توجه به معادله حالت:
[ PV = nRT ]
که در آن n، R و V ثابت و بدون تغییر هستند، رابطۀ فشار بر حسب دما مستقیم است، یعنی با افزایش دما، فشار نیز افزایش مییابد و با کاهش دما، فشار نیز کاهش مییابد.
فرآیند هم فشار
در این فرآیند فشار ثابت است. با توجه با رابطۀ معادله حالت حجم با دما نسبت مستقیم دارد. با افزایش دما، حجم نیز افزایش و با کاهش دما، حجم نیز کاهش مییابد.
در نمودار P-T در فرآیند هم فشار، به دلیل ثابت بودن فشار، نمودار به صورت افقی است. با افزایش دما، حجم نیز افزایش مییابد و با کاهش دما، حجم نیز کاهش مییابد.
در نمودار V-T در فرآیند هم فشار، امتداد نمودار به مبدأ میرسد زیرا عرض از مبدأ نمودار صفر است. شیب نمودار مقدار ( nRT/P ) است. با افزایش دما، حجم نیز افزایش مییابد.
در نمودار P-V در فرآیند هم حجم، با تغییر حجم، فشار دستگاه تغییر نمیکند و این نمودار افقی است. با افزایش دما، حجم افزایش و با کاهش دما، حجم کاهش مییابد. مساحت زیر این نمودار برابر با اندازه (قدر مطلق) کار انجام شده است.
فرآیند هم دما
در این فرآیند، دمای دستگاه ثابت است. از آنجایی که تغییر انرژی درونی یک گاز به دما وابسته است، انرژی درونی گاز نیز تغییر نمیکند؛ بنابراین، تغییر انرژی درونی گاز در این فرآیند صفر است.
با توجه به رابطه بین گرما، کار، و تغییر انرژی درونی گاز، در این فرآیند، مقدار گرمای مبادله شده، برابر با مقدار کار انجام شده است، با این تفاوت که علامت آنها معکوس است.
فرآیند بی دررو
در این فرآیند، دمای دستگاه ثابت است. از آنجایی که تغییرات انرژی درونی یک گاز به دما وابسته است، انرژی درونی گاز نیز ثابت میماند. بنابراین، تغییر انرژی درونی گاز در این فرآیند برابر با صفر است.
رابطه بین گرما، کار، و تغییر انرژی درونی گاز، در این فرآیند، مقدار گرمای مبادله شده با مقدار کار انجام شده برابر است.
با این تفاوت که علامت آنها معکوس است؛ کار انجام شده و گرمای مبادله شده دارای مقادیر معادل، اما با علایم مخالف هستند.
چرخۀ ترمودینامیکی
چرخه ترمودینامیکی یک دستگاه را هنگامی میگوییم. دستگاه چندین فرآیند را انجام داده و سپس به حالت اولیه خود بازگشته باشد. در واقع، یک چرخه ترمودینامیکی شامل توالیای از فرآیندها است که به حالت اولیه ختم میشود. به دلیل این بازگشت به حالت اولیه، تغییر انرژی درونی گاز در طول یک چرخه ترمودینامیکی، به صفر میرسد.
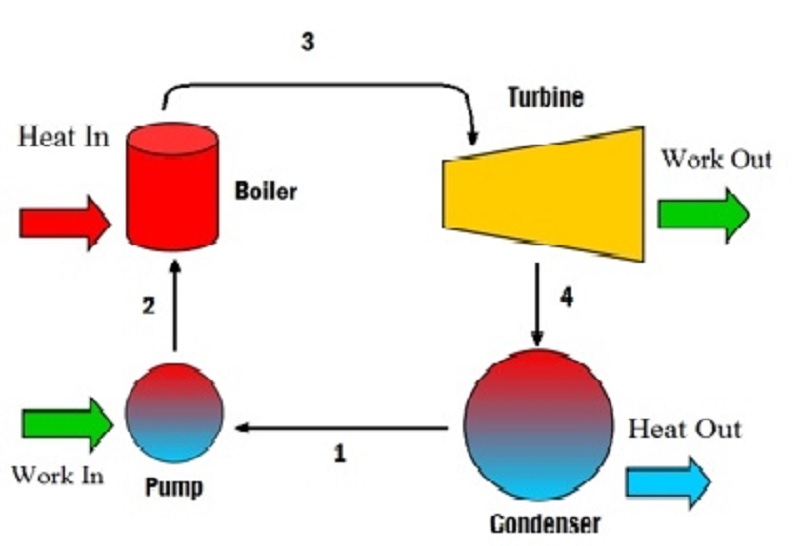
ماشین های گرمایی
یک ماشین گرمایی به هر دستگاهی اطلاق میشود که قادر باشد با استفاده از فرآیندهای ترمودینامیکی، انرژی حاصل از احتراق یا سوختن را به کاربرد مفیدی تبدیل کند.
انواع ماشین های گرمایی
تیپهای مختلف ماشینهای گرمایی
- ماشین گرمایی برونسوز: این دستگاهها منبع گرما را خارج از خود دارند؛ مثل ماشینهای بخار، ماشینهای نیوکامن و ماشینهای استرلینگ.
- ماشین گرمایی درونسوز: در این نوع ماشینها، منبع گرما در داخل دستگاه (گاز) قرار دارد؛ مانند موتورهای بنزینی و دیزل که در خودروها استفاده میشوند.
بازده ماشین گرمایی
نسبت انرژی مفید خروجی (کار انجام شده) به انرژی داده شده به ماشین
قانون دوم ترمودینامیک به بیان ماشین گرمایی
یک دستگاه چرخهای وجود ندارد که در طول آن تمامی گرمای جذب شده از منبع حرارت را به کار تبدیل کند. به عبارت دیگر، امکان داشتن بازدهی 100 درصد برای یک ماشین گرمایی وجود ندارد.
یخچال
وسیلۀ ای که با صرف کار، انرژی گرمایی را از منبع دما پایین می گیرد و به منبع دما بالا میدهد. به بیان ساده تر، وسیلۀ ای که با انجام کار، گرما را از جسمی سرد به جسمی گرم منتقل میکند.
قانون دوم ترمودینامیک به بیان یخچالی
یک پدیده معروف در فیزیک، اصل دوم ترمودینامیک، میگوید که انتقال گرما به طور خودبه خود از یک جسم با دمای پایینتر به یک جسم با دمای بالاتر امکانپذیر نیست. به عبارت دیگر، انرژی حرارتی به طور خودبخود از یک محیط سردتر به یک محیط گرمتر منتقل نمیشود، مگر با مداخله و اعمال کاری خارجی. این اصل به عنوان یکی از پایههای ترمودینامیک، درک فرآیندهای گرمایی و انتقال حرارت بین محیطهای مختلف را شرح میدهد و محدودیتهایی را برای تبادل حرارت مشخص میکند.


2 دیدگاه
به گفتگوی ما بپیوندید و دیدگاه خود را با ما در میان بگذارید.